SARS-CoV-2 中和抗体を測定するCLEIA試薬(STACIA®専用)
*本製品は研究用試薬です。
血清中のSARS-CoV-2に対する抗体の中和能の評価に
 本試薬は、スパイクとヒト受容体であるACE2との結合阻害活性を測定することにより、検体中のSARS-CoV-2に対する抗体の中和能を評価します。
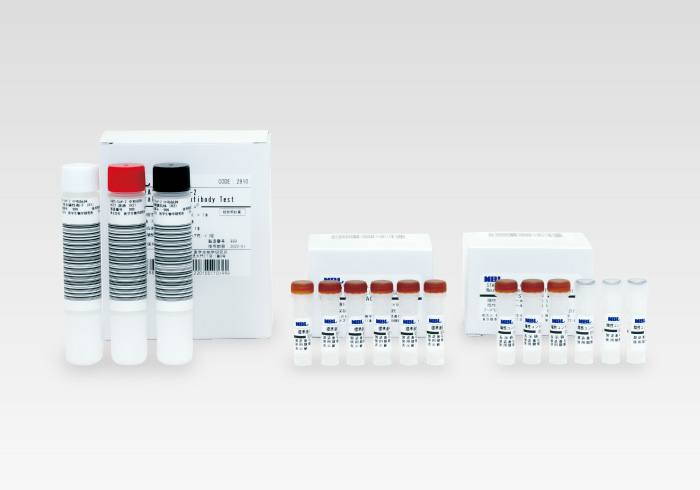
本試薬は、スパイクとヒト受容体であるACE2との結合阻害活性を測定することにより、検体中のSARS-CoV-2に対する抗体の中和能を評価します。
SARS-CoV-2は、ウイルス表面にあるスパイクがヒト細胞上の受容体であるACE2に結合することで細胞へ感染します。中和抗体によりスパイク-ACE2の相互作用が阻害されると、ウイルスはヒト細胞に感染できなくなります。(下記イラスト参照)
したがって、スパイク-ACE2相互作用の阻害の程度は、検体中のSARS-CoV-2に対する抗体の中和活性の指標となります。
試薬中のスパイク抗原としては、ACE2との結合領域である*RBDを使用しています。
製品概要・キット構成
| Code No. | 製品名 | 包装 | 保存温度 | 製品有効 |
|---|---|---|---|---|
| 2910 | STACIA® SARS-CoV-2 Neutralization Antibody Test |
100テスト | 2-8℃ | 6ヵ月 |
| キット構成 | RBD結合磁性粒子(R1) | 7 mL × 1本 | 付属品:専用開閉ボトルキャップ(ステイシア用) 3個 | |
| ACE2溶液(R2) | 7 mL × 1本 | |||
| 酵素標識抗体(R3) | 7 mL × 1本 | |||
関連製品(セット品)
| Code No. | 製品名 | 包装 |
|---|---|---|
| 2910-201 | STACIA® SARS-CoV-2 Neutralization Antibody Test Calibrators |
1 mL × 6濃度 各1本 |
| 2910-211 | STACIA® SARS-CoV-2 Neutralization Antibody Test Controls |
陽性コントロール 0.5 mL × 3本 陰性コントロール 0.5 mL × 3本 |
関連製品(別売)
| Code No. | 製品名 | 包装 |
|---|---|---|
| MC750083 | 基質液(R5)※1, ※2 | 125 mL × 1本 |
| MC750014 | 共通希釈液I(ステイシア用)※2 | 12 mL × 4本 |
| MC750076 | BF洗浄液(ステイシア用)※2 | 4 L × 1本 |
| MC750069 | アルカリ洗浄液(ステイシア用)※2 | 4 L × 1本 |
| MC750007 | リンス液(ステイシア用)※2 | 1 L × 1本 |
※1:体外診断用医薬品です。
※2:基質液(R5)、共通希釈液I(ステイシア用)、BF洗浄液(ステイシア用)、アルカリ洗浄液(ステイシア用)、リンス液(ステイシア用)及びキュベット(ステイシア用)はPHC株式会社が製造販売する試薬です。これらはPHC株式会社の全自動臨床検査システム「STACIA®」で測定項目に共通して使用する試薬です。
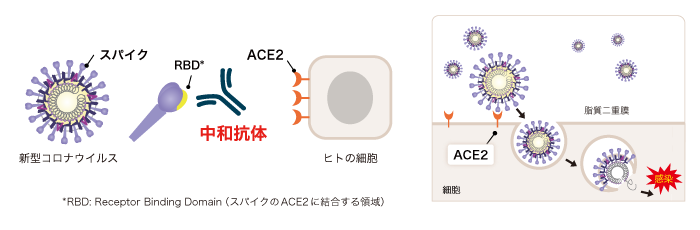
測定原理・測定フロー
本製品は、CLEIAを原理として血清中の抗SARS-CoV-2抗体によるウイルスのスパイクタンパク質の受容体結合ドメイン(RBD)とヒト細胞受容体(ACE2)の相互作用に対する阻害効果を測定します。
患者検体※と健常人検体の分布
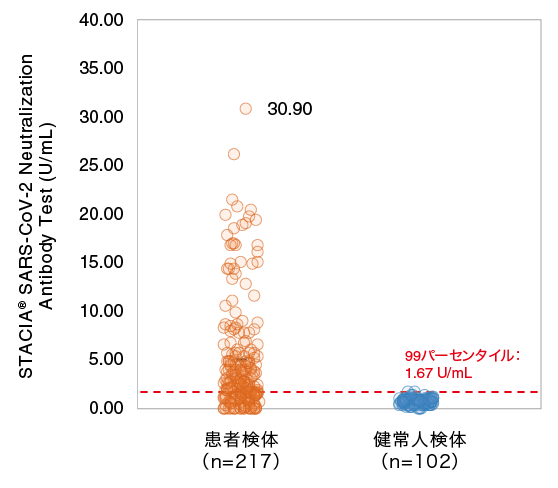 健常人の血清検体102例と新型コロナウイルスに感染した患者の検体217例を本試薬で測定した結果です。
健常人の血清検体102例と新型コロナウイルスに感染した患者の検体217例を本試薬で測定した結果です。
患者検体は、診断された時点より約1か月経過後に採血しました。
健常人検体の99パーセンタイル値は1.67 U/mLで、1.67 U/mL以上の検体は2/102検体(1.69%)でした。
患者検体では、約7割が2.00 U/mL以上となり、最大値は30.90 U/mLでした。
※本研究で用いた検体はワクチン接種者由来ではありません。
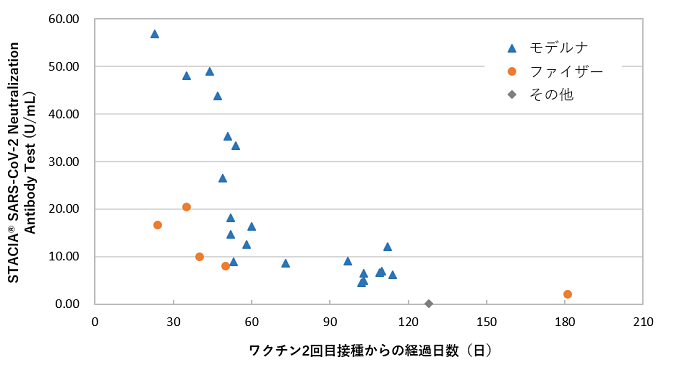
ワクチン接種後の測定例
ワクチン2回接種者の検体27例の中和抗体活性を本試薬で測定しました。
以下のグラフは2回目接種からの経過日数に対して測定値をプロットした結果となります。
ウイルス中和試験との相関
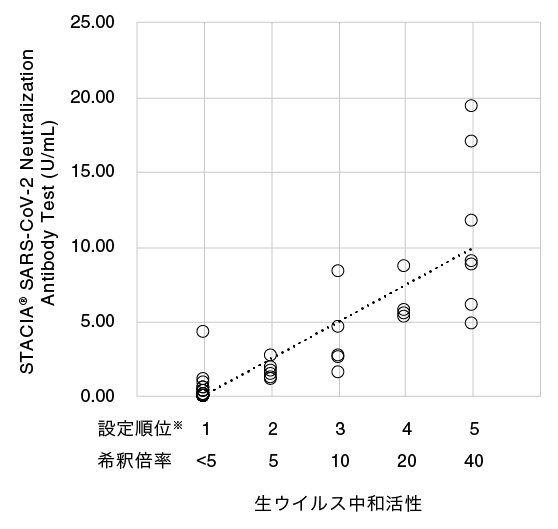 ウイルス中和試験の力価が明らかな血清検体43例を本試薬で測定しました。
ウイルス中和試験の力価が明らかな血清検体43例を本試薬で測定しました。
本試薬の測定結果と#ウイルス中和試験の結果は良好な相関を示しました。
(Spearman’s rank correlation test; rs=0.906, p<0.0001)
本キットにより、簡便に患者検体のウイルス中和活性を評価できることを確認しました。
#ウイルス中和試験
国立感染症研究所で確立したプロトコールに従い、Vero-E6/TMPRSS細胞をウイルス感染細胞として中和試験を実施しました。
中和が確認された最大検体希釈倍率を中和力価として評価しました。
※生ウイルス中和活性(希釈倍率)5倍未満を順位1、5倍を順位2、10倍を順位3、20倍を順位4、40倍を順位5として設定しました。