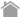DDDDK融合タンパク質精製ゲル~実践編~

 他社製品との性能比較
他社製品との性能比較 10回再利用テスト(非還元条件下)
10回再利用テスト(非還元条件下) 10回再利用テスト(還元条件下)
10回再利用テスト(還元条件下) pH3.0耐性テスト
pH3.0耐性テスト 他社製品との性能比較
他社製品との性能比較
2種類のタンパク質の精製度比較
DDDDK-tagged PROTEIN PURIFICATION GEL(Code No.3328)とA社精製ゲルを用いて、DDDDK-tagのついた2種類のタンパク質をバッチ法により精製しました。
プロトコール

DDDDKタグ融合タンパク質精製量・カラムへの残存量比較
ペプチド溶出後のDDDDK融合タンパク質量と、溶出後のビーズに残ったタンパク質量をゲル電気泳動およびクマシー染色を行い比較しました。
実験条件
ゲル: DDDDK-tagged PROTEIN PURIFICATION GEL(Code No.3328)、A社ゲルを各5 μL(ゲル容量)使用
精製前サンプル:RPMI/ 10% FCS 0.5 mL+ 5 mg DDDDK-GFP
RPMI/ 10% FCS 0.5 mL+ 5 mg DDDDK-BAP
精製前サンプルとゲルの反応時間:4°C 1時間
溶出:DDDDK-tag peptide(Code No.3325-205)20 μL×2回
泳動サンプル:ペプチド溶出サンプル40 μL中、20 μL泳動したもの(サンプル)
溶出後のゲルにSDS-PAGEバッファー20 μLを加え煮沸し、20 μL泳動したもの(ゲルへの残存)
高塩濃度下におけるMBLゲルと他社ゲルとの精製量比較
DDDDKタグ融合GFPタンパク質の精製
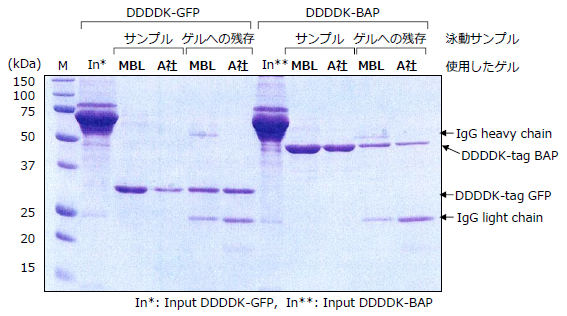
DDDDK-tagged PROTEIN PURIFICATION GEL(Code No.3328)とA社精製ゲルを用いて、3種類のバッファーで精製量を比較しました。
実験条件
サンプル:DDDDK-tagged GFP 10 μg/ sample
ゲル: DDDDK-tagged PROTEIN PURIFICATION GEL(Code No.3328)、A社ゲルを各10 μL(ゲル容量)使用
溶出:DDDDK-tag peptide(Code No.3325-205)20 μL×2回
溶出後サンプルを各20 μL泳動
DDDDKタグ融合β-Galactosidaseタンパク質の精製
DDDDK-tagged PROTEIN PURIFICATION GEL(Code No.3328)とA社精製ゲルを用いて、3種類のバッファーで精製量を比較しました。
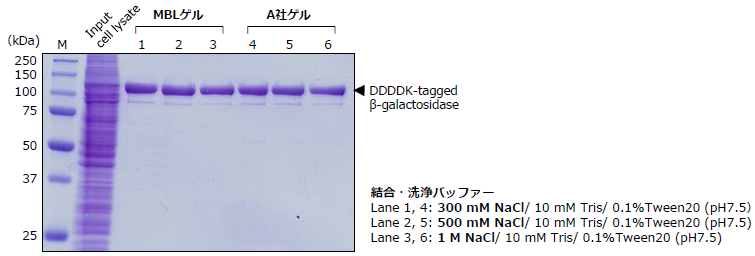
実験条件
サンプル:DDDDK-tagged β-galactosidase/ 293T TF cell lysate (2x106 cells/sample)
ゲル: DDDDK-tagged PROTEIN PURIFICATION GEL(Code No.3329)、A社ゲルを各10 μL(ゲル容量)使用
溶出:DDDDK-tag peptide(Code No.3325-205)20 μL×2回
溶出後サンプルを各20 μL泳動
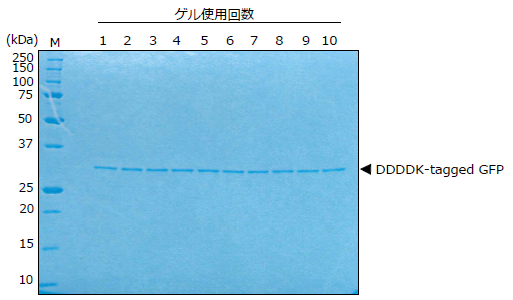
 10回再利用テスト(非還元条件下)
10回再利用テスト(非還元条件下)
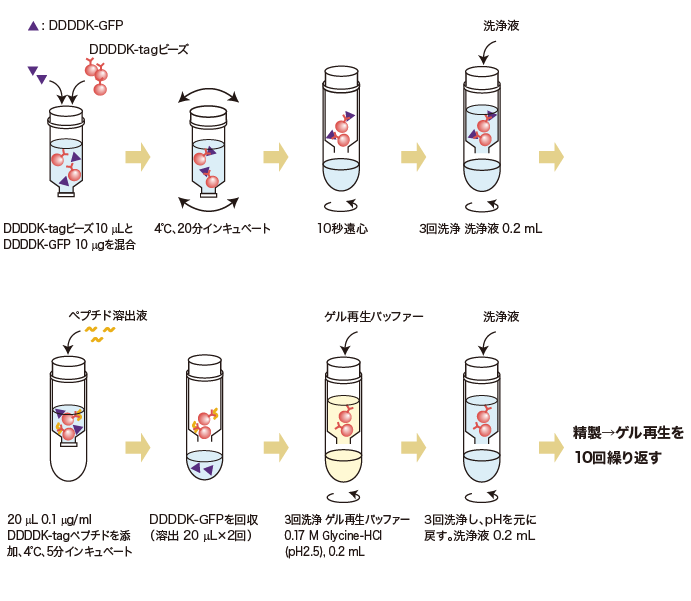
DDDDK-tagged PROTEIN PURIFICATION GEL(Code No. 3328)を用いてDDDDKタグ融合GFPタンパク質(DDDDK-GFP)の精製・溶出を行った後、ゲル再生バッファーにてゲルの再生を行いました。このゲルを用いて同様にDDDDK-GFPの精製・溶出を行い、この操作を10回繰り返しました。
再生テストプロトコール
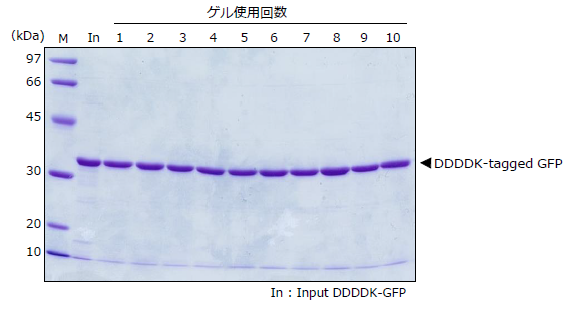
精製したDDDDKタグ融合GFPタンパク質の量比較
溶出液40 μL中、20 μLを12.5%アクリルアミドゲルで電気泳動し、クマシー染色を行いました。
再利用10回目でも1回目と同量のタンパクを回収できています。
 10回再利用テスト(還元条件下)
10回再利用テスト(還元条件下)
DDDDK-tagged PROTEIN PURIFICATION GEL(Code No.3328)を用いて1 mM DTTまたは10 mM 2-メルカプトエタノール(2-ME)存在下でタンパク質精製を行った後、ゲル再生バッファーにてゲルの再生を行いました。このゲルを用いて同様にDDDDK-GFPタンパク質の精製・溶出を行い、この操作を10回繰り返しました。
再生テストプロトコール

精製したDDDDKタグ融合GFPタンパク質の量比較
溶出液40 μL中、10 μLを12.5%アクリルアミドゲルで電気泳動し、クマシー染色を行いました。
10 mM DTT、10 mM 2-MEいずれの還元条件下でも、再利用10回目で1回目と同量のタンパク質を回収できました。
10 mM DTTを含有した結合液、洗浄液、溶出液を使用
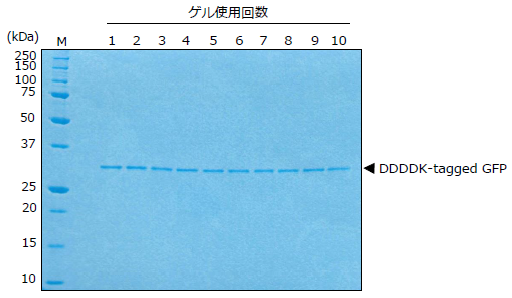
10 mM 2-MEを含有した結合液、洗浄液、溶出液を使用
 pH3.0耐性テスト
pH3.0耐性テスト
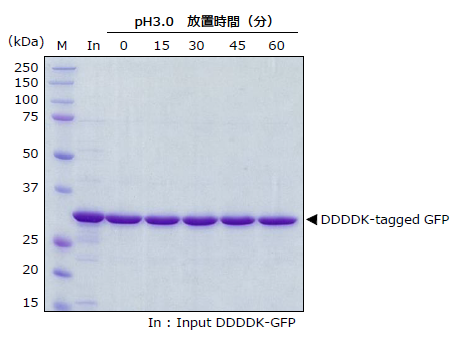
DDDDK-tagged PROTEIN PURIFICATION GEL(Code No.3328)をグリシンバッファー(pH3.0)と混合して15、30、45、60分インキュベートした後、DDDDKタグ融合GFPタンパク質(DDDDK-GFP)の精製・溶出を行った時の精製量を比較検討しました。
pH3.0耐性テストプロトコール
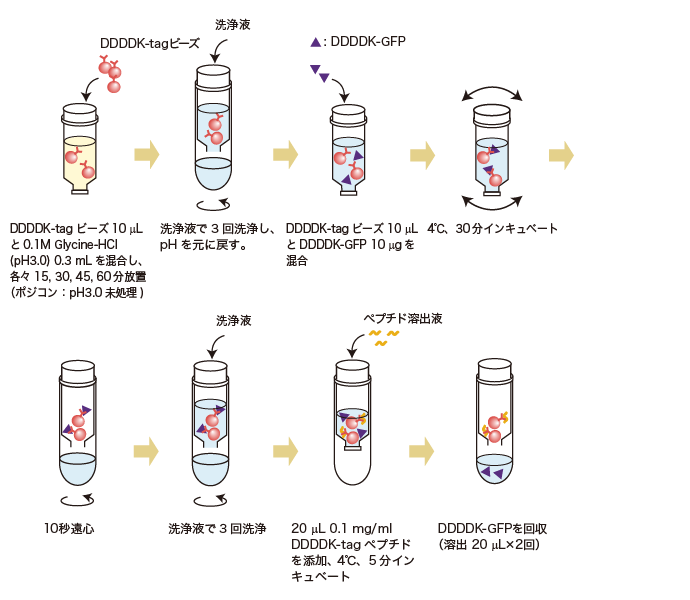
精製したDDDDKタグ融合GFPタンパク質の量比較
溶出液40 μL中、20 μLを12.5%アクリルアミドゲルで電気泳動し、クマシー染色を行いました。
pH3.0のバッファーに60分放置したゲルでも、pH3.0未処理のゲルと同量のタンパクを回収できました。