Qkine社のFGF2-G3
熱安定性に優れる高活性FGF2

特長
幹細胞培養に広く利用されているFGF2は、細胞培養液中で分解や凝集体を形成して十分に活性を発揮できず、幹細胞の増殖や増殖後の分化の均一性において課題となっていました。
FGF受容体との結合能には影響がなく、安定化に最適な9つのアミノ酸を置換した改変型FGF2「FGF2-G3」は、生物活性は野生型と同等で、熱安定性が大きく向上しています。
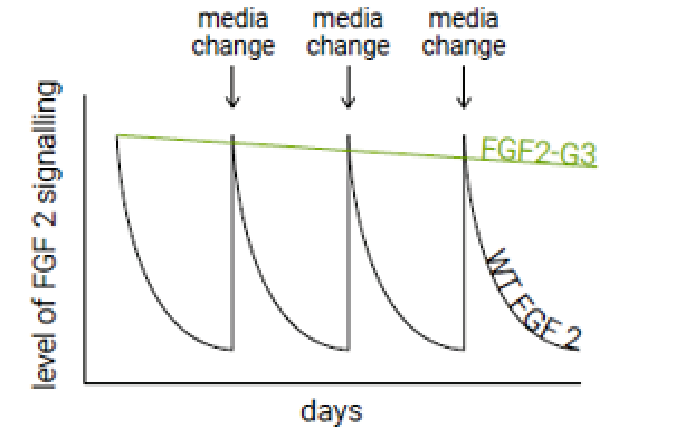
細胞培養におけるFGF2の半減期は10時間未満であり頻繁な培地交換が必要ですが、FGF2-G3は、半減期が3日を超えるためウィークエンドフリープロトコルに適用可能です。
Qkine社では、以下の2種類のFGF2-G3製品を用意しています。
・145 aa FGF2-G3(QK052)
・154 aa FGF2-G3(QK053)
半減期が3日を超えるため、ウィークエンドフリープロトコルに適用可能です。
FGF2-G3の基本データ
アイソフォーム① :FGF2-G3 145 aa(QK052)
■ ルシフェラーゼレポーターアッセイ
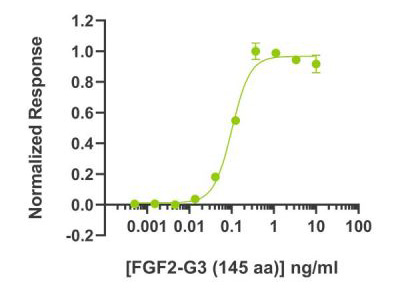
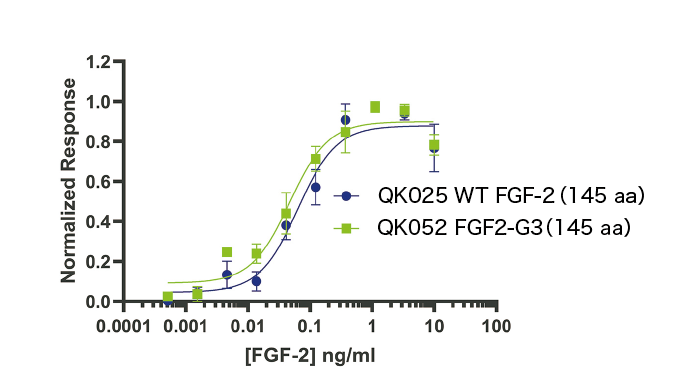
FGF2-G3 145 aa(QK052)をルシフェラーゼレポーターアッセイを用いて生物活性を測定したところ、EC50は101 pg/ml(6.2 pM)でした。
■ 純度(15% w/v SDS-PAGE[還元(R)、非還元(NR)])
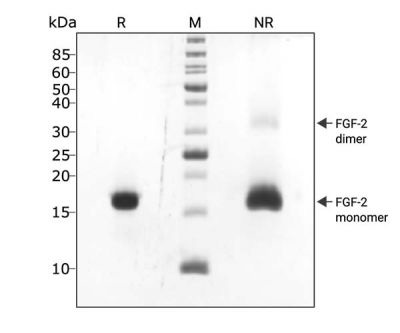
FGF2-G3 145 aa(QK052)を、SDS-PAGEを使用して分離し、CBBで染色しました。 FGF2-G3 145 aa (QK052)は、非還元条件で16kDaの主要バンドとして移動し、少量の二量体が検出される一方で、還元条件では、16kDaのバンドのみが観察されました。
アイソフォーム② :154 aa FGF2-G3(QK053)
■ ルシフェラーゼレポーターアッセイ
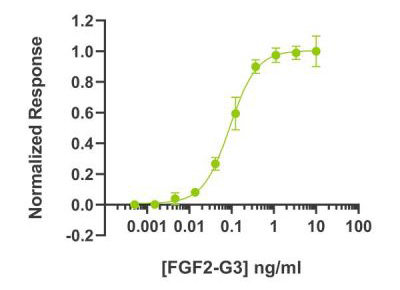
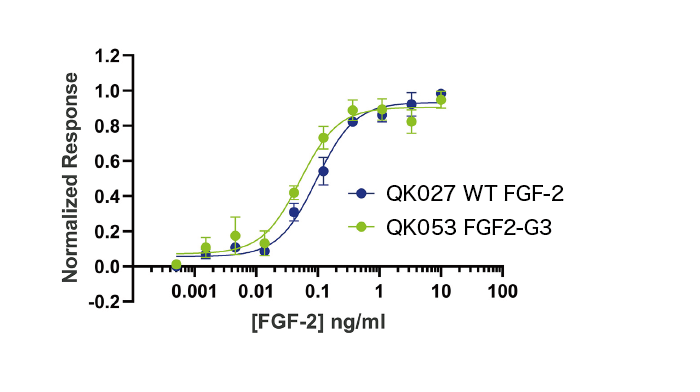
FGF2-G3(QK053)をルシフェラーゼレポーターアッセイを用いて生物活性を測定したところ、EC50は90 pg/ml(5.2 pM)でした。
■ 純度(15% w/v SDS-PAGE[還元(R)、非還元(NR)])
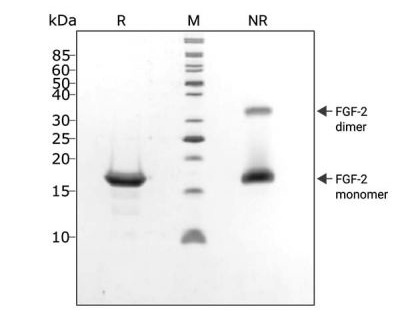
FGF2-G3(QK053)を、SDS-PAGEを使用して分離し、CBBで染色しました。FGF2-G3(QK053)は、非還元条件で17kDaの主要バンドとして移動し、高分子量のマイナーバンドとして二量体が検出されました。還元条件では、17kDaのバンドのみが観察されました。
野生型FGF2と改変型FGF2-G3は同等の生物活性を示します
アイソフォーム① 145 aa
アイソフォーム② 154 aa
FGF2-G3 は、37℃で培養した後も活性を維持します
アイソフォーム① 145 aaのルシフェラーゼレポーターアッセイ結果
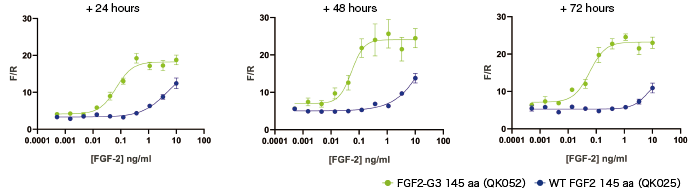
アイソフォーム② 154 aaのルシフェラーゼレポーターアッセイ結果
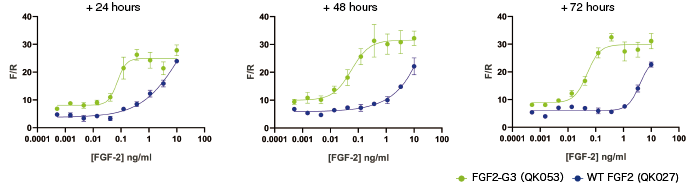
野生型FGF2とFGF2-G3を馴化培地で希釈し、37℃で培養しました。サンプルを24時間間隔で採取して段階的に希釈した後、ルシフェラーゼレポーターアッセイによる生物活性評価を行いました。野生型FGF2は処理時間とともに活性が低下しましたが、FGF-G3は72時間処理後でも活性が損なわれることなく維持されました。
FGF2-G3 製品仕様
| Code | Product | species reactivity | 50 µg | 100 µg | 500 µg | 1000 µg |
|---|---|---|---|---|---|---|
| QK052 | FGF2-G3(145 aa) | species neutral | ✓ | ✓ | ✓ | ✓ |
| QK053 | FGF2-G3 | species neutral | ✓ | ✓ | ✓ | ✓ |
参考文献
- FGF2-G3 was developed by Dvorak et al., Biotechnology and Bioengineering 115: 850-862 (2018)
- B8 media protocol established by Kuo et al., Stem Cell Reports 14: 256-270 (2020)
- B8 media protocol updated in Lyra-Leite et al., 2021. STAR Protocols 2: 100213 (2021)
- review of FGF 2 stabilization by Benington et al., Pharmaceutics 12: 508 (2020)
Qkine社について
Qkine社は、2016年にケンブリッジ大学のMarko Hyvönen博士の研究室から独立し設立されました。
Marko Hyvönen博士の研究室で開発された独自の製造プロセスとタンパク質工学技術を組み合わせて、生物活性を有する高純度のアニマルフリーのリコンビナントタンパク質を製造しています。
Qkine社のリコンビナントタンパク質は、すべてQkine社の動物由来成分フリー(ADCF)ラボで製造され、非常に厳格で堅牢な品質管理基準に合格した製品を提供することにより、幹細胞、細胞小器官、再生医療分野の研究開発をサポートしています。